コロナワクチンのスパイクタンパク病原性に対するターメリック、活性成分クルクミンの抑制効果に注目!
と遺伝子(赤平)-e1720326162405.jpg)
新型コロナウイルスのスパイクタンパク質は、ウイルスのみならず、そのタンパク質自体が持つ病原性(毒性)が、コロナ遺伝子ワクチン後遺症において様々な疾患を招いてしまう。

今回は、コロナ遺伝子ワクチン後遺症が、私たちの身体にいつまでも棲み続けしまうスパイクタンパクについてPubMed(米国国立医学図書館 国立衛生研究所)に寄せられている報告を交えながら、その内容をお伝えしたいと思うとるんじゃ!

コロナ遺伝子ワクチンがスパイクタンパクをいつまでも作りつづけるって、どういうこと?

詳しくは、ちょっと複雑なので、ある機関の記述を参考に説明させてもらいたい!
コロナウイルスとコロナワクチンmRNA由来スパイクタンパクの病原性
新型コロナウイルスに対する遺伝子ワクチンの接種によって、様々な副反応や後遺症が起き、社会問題となっています。
特に副反応はアナフィラキシーショックだけでなく、ワクチン接種後に脳卒中、心筋梗塞、心筋炎、そして因果関係を確定できない多数の死亡例が報告されています。
さらに、ワクチン接種後に倦怠感、慢性疲労、頭痛、ブレインフォグ、脱毛、息切れ、胸痛、動悸、うつ症状、しびれ、めまい、じんま疹、月経異常、歩行障害など様々な症状が長期に続くケースも増加しています。
これらはワクチン後遺症、あるいはワクチン接種後症候群とも呼ばれていますが、治療法が確立されていません。
スパイクタンパクがワクチン後遺症の病因に深く関わっている
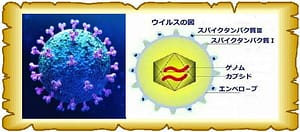
スパイクタンパクはコロナウイルスの表面にある突起で、細胞膜上のアンジオテンシン変換酵素2(ACE2受容体)に付着して細胞内に侵入します。
新型コロナ遺伝子ワクチンはmRNAを接種することで、スパイクタンパク質を作るようにプログラムされています。
本来は、ウイルスから身体を守るための免疫反応を引き起こすように設計され、役目が終われば、分解されるはずのRNAがコロナ遺伝子ワクチンでは分解されないように改造されており、結果、抗体がつくられるプロセスが継続したままになってしまうことが明らかにされています。
人工遺伝子が半永久的に残り、新種のスパイクタンパクが生成され、そのタンパクに対する抗体反応が永遠に続くことが、深刻な問題であると、岡田正彦 新潟大学名誉教授によって早くから指摘されています。
当初は接種部位の筋細胞のみでスパイクタンパクが作られると公表されていたが、肝臓、骨髄、卵巣など全身の細胞にワクチンのRNAが拡散され、スパイクタンパクが作られていることが分かってきました。
そして、このスパイクタンパクが組織や臓器全体に炎症と凝固を引き起こす可能性があることも報告されています。
全身の細胞でスパイクタンパクが作られることで、 実は自分の免疫システムが過剰に働き、サイトカインストームを誘発、自身を攻撃することになってしまいます。
血管内皮細胞を始め、様々な細胞や臓器を傷つけ、血栓症、ブレインフォグ、組織性肺炎、心筋炎などの疾患をまねき、多くのワクチン後遺症に苦しんでみえる方々が、時の経過とともに増え続けているようです。
ウイルスとワクチン両方のmRNAによるスパイクタンパクの病原性(毒性)を認めたPubMed(米国国立医学図書館 国立衛生研究において、報告がなされています。
コロナ感染症のスパイクタンパク質はウイルスとワクチンmRNAの両方に病原性がある
PubMed(米国国立医学図書館 国立衛生研究所)
2023年8月17日;11(8):2287.
所属
クイーンズランド大学医学部、小児健康研究臨床ユニット、及びフリンダース大学医学・公衆衛生学部精神医学科、オーストラリア。
概略
「安全で効果的な」ワクチンの製造は、公衆衛生上の重要な目標でしたが、悲しいことに、前例のない高い有害事象率がその効果を覆い隠しています。
レビューでは、新製品のCOVID-19 mRNAワクチンとアデノベクターDNAワクチンの広範な害の証拠を提示し、病原性の証拠がある外来抗原を生成するヒト細胞に依存するワクチンの新技術から生じる害の徹底的な概要を提供しようとする点で斬新です。
この最初の論文では、これらの新技術に付随する「安全で効果的」な物語に反する査読済みデータを調査します。
SARS-CoV-2ウイルス由来であれ、「合成ウイルス」に似たワクチン遺伝子コードによって生成されたものであれ、「スパイクオパシー」と呼ばれるスパイクタンパク質の病原性は、分子生物学と病態生理学の観点からますます明白になっています。
脂質ナノ粒子またはウイルスベクターキャリアによる、薬物動態学的トランスフェクションは、「スパイク病」が多くの臓器に影響を及ぼす可能性があることを意味します。
mRNA を輸送するために使用されるナノ粒子の炎症特性、合成 mRNA の機能を延長するために使用される N1-メチルシュードウリジン、mRNA および DNA コードと翻訳されたスパイクタンパク質の広範な生体内分布、およびヒトによる外来タンパク質の生成による自己免疫は、有害な影響の一因となります。
スパイク病の自己免疫、心血管、神経、潜在的な腫瘍学的影響、および剖検証拠についてレビューします。多くの遺伝子ベースの治療技術が計画されている再評価は必要かつタイムリーです。
体内に残されたスパイクタンパクを解毒することはワクチン後遺症の治療にとって最も大切なことになります。
コロナ遺伝子ワクチンによって半永久といわれる身体の中にあるmRNAによるスパイクタンパクを確実に分解し、排泄させる方法が求められています。
ワクチン後遺症治療・スパイクタンパク病原性(毒性)のデトックスにターメリック、活性成分クルクミンの抑制効果!
ターメリック活性成分クルクミンのスパイクタンパク抑制効果についてPubMed(米国国立医学図書館 国立衛生研究所)の研究報告を掲載します。
クルクミンとCOVID-19タンパク質の分子ドッキングとダイナミクス研究
PubMed(米国国立医学図書館 国立衛生研究所)
2021;10(1):44.
所属
マニパル大学ジャイプール校化学学部、ジャイプール、303 007 ラジャスタン州インド。
バイオテクノロジー部門、ヴィニャン科学技術研究財団、アーンドラ・プラデーシュ州、インド。
コロナウイルス病 2019 (COVID-19) は、プラス鎖 RNA ウイルスである重症急性呼吸器症候群コロナウイルス 2 (SARS-CoV-2) によって引き起こされます。
SARS-CoV-2 ゲノムと SAR-CoV-1 との関連性は、ベータコロナウイルス科のメンバーの種類に応じて約 66% から 96% まで異なります。
クロロキン、ヒドロキシクロロキン、イベルメクチン、アルテミシニン、レムデシビル、アジスロマイシンなど、いくつかの薬剤が臨床試験で検討されているため、これらの薬剤の独特の抗ウイルスメカニズムを見つける必要性が本質的にありました。
天然の生理活性分子であるクルクミンは、さまざまな疾患の治療効果があることが示されており、COVID-19 に対するその効果も現在調査されています。
この研究では、さまざまな SARS-CoV-2 タンパク質を標的としたクルクミンの結合可能性を示します。
スパイク糖タンパク質(PDB ID:6VYB)、ヌクレオカプシドリン酸化タンパク質(PDB ID:6VYO)、スパイクタンパク質ACE2(PDB ID:6M17)に加えて、nsp10(PDB ID:6W4H)およびRNA依存性RNAポリメラーゼ(PDB ID:6M71)構造。
さらに、代表的なドッキング複合体は分子動力学シミュレーションを使用して検証され、100 nsでの機構研究がクルクミン複合体とヌクレオカプシドおよびnsp10タンパク質に対して実施され、安定した効率的な結合エネルギーが得られ、複合体のドッキング結合エネルギーと相関しました。
ドッキング研究とシミュレーション研究の両方から、クルクミンはCOVID-19に対する抗ウイルス剤としての可能性があることが示されています。
COVID-19の制御のための抗菌光線力学療法の可能性に関する分子モデリングとシミュレーション分析
PubMed(米国国立医学図書館 国立衛生研究所)
2022年5月31日:2022:7089576。
所属
イラン、テヘラン、テヘラン医科大学、歯科研究所、歯科研究センター。
重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)は、ウイルス表面スパイク糖タンパク質(SG)をアンジオテンシン変換酵素2に結合させることで宿主細胞に侵入することができます。
抗ウイルス光線力学療法(aPDT)はウイルス感染を阻害する新しい方法として説明されているため、COVID-19を制御するための光活性化消毒剤として使用できるかどうかを評価することが重要です。
このin silico研究では、SARS-CoV-2-SGがaPDT中の光増感剤としてのクルクミンの新しいターゲットとして選択され、その物理化学的特性、分子モデリング、タンパク質構造の階層的性質、およびいくつかのバイオインフォマティクスツールと生物学的データベースを使用した機能分析が活用されました。
詳細な計算調査の結果、SARS-CoV-2-SGは6VXX_Aに最も類似しており、クエリカバー率と同一性が100%であることが明らかになりました。
SARS-CoV-2-SGの予測構造は、正電荷を持つタンパク質であり、ランダムコイルがウイルス細胞の外側にある他の二次構造を支配していることを示しました。
タンパク質間相互作用ネットワークは、SARS-CoV-2-SGが10の潜在的な相互作用パートナーと相互作用することを示しました。
さらに、分子ドッキングによる結合モードの一次スクリーニングにより、クルクミンはaPDTの収量を高めるための主な部位としてSARS-CoV-2-SGの残基と結合して相互作用することを望んでいることが示されました。
全体として、コンピューターシミュレーションは、SARS-CoV-2-SGがaPDT中にクルクミンと相互作用するための適切なターゲット部位になり得ることを明らかにしました。
COVID-19関連主要酵素に対する潜在的候補としての新しいクルクミン誘導体の設計と様々なin silico研究
PubMed(米国国立医学図書館 国立衛生研究所)
2022年6月:98:107657。
所属
ゾングルダク・ビュレント・エジェヴィト大学文学部物理学科、67100 ゾングルダク、トルコ。電子メールアドレス: hakanalici@beun.edu.tr。
カラビュク大学理学部化学科、78050 カラビュク、トルコ。
新型コロナウイルス感染症(COVID-19)は、SARS-CoV-2ウイルスによって引き起こされる非常に伝染性の高い疾患で、患者に重度の急性呼吸器症候群を引き起こします。
これまでSARS-CoV-2に対してさまざまな抗ウイルス薬とその組み合わせが試され、ある程度の有効性を示していますが、COVID-19との戦いには安全で費用対効果の高い結合阻害剤が依然として必要とされています。
したがって、自然界の植物化学物質は、その幅広い治療スペクトルと強力な抗ウイルス、抗炎症、抗酸化特性により、迅速な解決策となり得ます。
この文脈において、天然植物化学物質であるクルクミンの低毒性と高い薬物動態特性、およびその誘導体の容易な合成は、コロナウイルスに対する阻害剤としてのさまざまな誘導体の研究の必要性を示しています。
本研究では、信頼性の高いADMEプロファイルと、さまざまなSARS-CoV-2標的酵素(3CLPro、PLpro、NSP7/8/12、NSP7/8/12 +RNA、NSP15、NSP16、Spike、Spike+ACE)に対する高い分子結合能を持つクルクミン誘導体に焦点を当てました。
分子ドッキング研究では、提案された22のクルクミン誘導体の最高の結合スコアがPLproタンパク質に対して得られました。
さらに、高親和性リガンド-PLproタンパク質複合体のMDシミュレーションを実行し、続いてPLproのLys157、Glu161、Asp164、Arg166、Glu167、Met208、Pro247、Pro248、Tyr264、Tyr273、およびAsp302残基が分子力学ポアソンボルツマン表面積(MM-PBSA)分析によってリガンド結合に重要な役割を果たすことが判明しました。
この研究の結果は、提案されたクルクミン誘導体がSARS-CoV-2に対する強力な阻害剤となり、医薬品に変換できることを示唆しています。
また、この発見は、植物化学物質のさまざまな抗ウイルス誘導体を合成するための将来の設計研究に指針となる洞察を提供するものと期待されています。
SARS-CoV-2およびSARS-CoVのスパイク表面糖タンパク質に対するクルクミンとその類似体の仮想スクリーニング
PubMed(米国国立医学図書館 国立衛生研究所)
2022年7月;40(11):5138-5146.
所属
インド、グジャラート州チャンガ、チャロタール科学技術大学、ラマンバイ・パテル薬学部。
インド、カルナタカ州バンガロール、インドアカデミーディグリーカレッジ - オートノマス、生化学科。
COVID-19は、SARS-CoV-2によって引き起こされる新たなパンデミックであり、2019年に中国の武漢で初めて特定されました。
新型コロナウイルスSARS-CoV-2と2002年のSARS-CoVは74%の同一性があり、細胞に侵入するための同様のメカニズムを使用します。
両方のウイルスは、ウイルススパイク糖タンパク質が宿主受容体であるアンジオテンシン変換酵素2(ACE2)に結合することで宿主細胞に侵入します。
ウイルスの侵入を標的とすることは、ウイルスライフサイクルの後期段階を阻害するよりも有利です。
SARS-CoV(6CRV:全長Sタンパク質)とSARS-CoV-2スパイクタンパク質(6M0J:受容体結合ドメイン、RBD)の結晶構造を使用して、潜在的な低分子阻害剤を特定しました。
ウコンに天然に存在する植物化学物質であるクルクミンは、幅広い薬理特性を持つことが知られています。
本研究では、Autodock 4.2 を使用してクルクミンとその誘導体を 6CRV と 6M0J にドッキングし、スパイクタンパク質の阻害剤として作用してウイルスの侵入を阻止する能力を研究しました。
クルクミンとその誘導体の結合エネルギー ΔG は、-10.98 ~ -5.12 kcal/mol (6CRV) および -10.01 ~ -5.33 kcal/mol (6M0J) の範囲でした。
結合エネルギーが最も低かったのはビスデメトキシクルクミンで、ΔG = -10.98 kcal/mol (6CRV) および -10.01 kcal/mol (6M0J) でした。
良好な結合エネルギー、薬物類似性、効率的な薬物動態パラメータは、クルクミンとそのいくつかの誘導体が SARS-CoV-2 スパイクタンパク質阻害剤になる可能性があることを示唆しています。
Ramaswamy H. Sarma による報告。
-1-e1653658302258.jpg)